Gestion des risques associés à la possibilité de double usage dans la recherche en sciences de la vie
Table des matières
- Préface
- Abréviations et sigles
- Chapitre 1 – Introduction
- Chapitre 2 – Possibilité de double usage
- Chapitre 3 – Processus de gestion des risques
- Chapitre 4 – Opportunités de gestion des risques tout au long d'un projet de recherche
- Chapitre 5 – Références et ressources
- Annexe A – Initiatives internationales relatives à la possibilité de double usage
Préface
Au Canada, les installations où sont manipulés et entreposés des agents pathogènes humains de groupe de risque 2 (GR2), GR3 et GR4 ou des toxines réglementées sont réglementées en vertu de la Loi sur les agents pathogènes humains et les toxines (LAPHT) et du Règlement sur les agents pathogènes humains et les toxines (RAPHT). La manipulation et l’entreposage d’agents zoopathogènes importés de GR2, GR3 et GR4 ou de parties de ceux-ci (p. ex. une toxine) sont réglementés en vertu de la Loi sur la santé des animaux (LSA) et du Règlement sur la santé des animaux (RSA).
En vertu de la LAPHT et du RAPHT, l’Agence de la santé publique du Canada (ASPC) réglemente la manipulation et l’entreposage d’agents pathogènes humains et de toxines. De plus, en vertu de la LSA et du RSA, l'ASPC réglemente l'importation et le transfert ou la réception subséquents d'agents pathogènes indigènes d'animaux terrestres ou de parties de ceux-ci en culture pure ou dans des matrices ne provenant pas d’animaux (p. ex. un échantillon humain, végétal, alimentaire ou environnemental).
L’Agence canadienne d’inspection des aliments (ACIA) réglemente l’importation et le transfert ou la réception subséquents des autres agents zoopathogènes ou de parties de ceux-ci (p. ex. une toxine) en vertu de la LSA et du RSA. Cela comprend les agents pathogènes d’animaux terrestres désignés par l’ACIA (APAT-DA), tout agent pathogène d’animaux terrestres présent dans des animaux, des produits animaux et des sous-produits animaux (p. ex. des tissus, du sérum), les agents pathogènes des abeilles et les agents pathogènes d’animaux aquatiques. Le terme « APAT-DA » comprend les maladies animales exotiques (MAE), les maladies animales émergentes (MAÉ) et les agents pathogènes non indigènes d’animaux terrestres relevant de la compétence de l'ACIA.
La figure suivante illustre la hiérarchie des documents qu'utilisent l'ASPC et l'ACIA pour surveiller les activités de biosécurité et de biosûreté. Chaque niveau de la pyramide correspond à un type de document. Les documents sont placés en ordre de priorité du haut de la pyramide vers le bas. Les lois et les règlements se trouvent au sommet de la pyramide, car ce sont ces documents qui confèrent à l'ASPC et à l'ACIA leur autorité légale. Les outils de communication des risques et les documents techniques sont à la base de la pyramide, puisqu'ils visent seulement à résumer les recommandations et l’information scientifique.
La ligne directrice Gestion des risques associés à la possibilité de double usage dans la recherche en sciences de la vie a été élaborée par l'ASPC et l'ACIA dans le cadre d'une série de publications électroniques qui portent sur les concepts de biosécurité et de biosûreté abordés dans la Norme canadienne sur la biosécurité, troisième édition (NCB). La présente ligne directrice fournit des renseignements et des considérations sur la manière d'évaluer la possibilité de double usage dans la recherche en sciences de la vie impliquant des agents pathogènes, des toxines ou d'autres matières biologiques, et sur la manière de gérer les risques associés.
Retour en hautAbréviations et sigles
|
Abréviation |
Terme |
|---|---|
|
ABCSE |
Agent biologique à cote de sécurité élevée |
|
ACIA |
Agence canadienne d'inspection des aliments |
|
AMC |
Affaires mondiales Canada |
|
APAT-DA |
Agent pathogène d'animaux terrestres désigné par l'Agence canadienne d'inspection des aliments |
|
ASB |
Agent de la sécurité biologique |
|
ASFC |
Agence des services frontaliers du Canada |
|
ASPC |
Agence de la santé publique du Canada |
|
CIB |
Comité institutionnel de biosécurité |
|
GR |
Groupe de risque (c.-à-d. GR1, GR2, GR3, GR4) |
|
GRC |
Gendarmerie royale du Canada |
|
IA |
Intelligence artificielle |
|
LAPHT |
Loi sur les agents pathogènes humains et les toxines |
|
LSA |
Loi sur la santé des animaux |
|
NC |
Niveau de confinement (c.-à-d. NC1, NC2, NC3, NC4) |
|
NCB |
Norme canadienne sur la biosécurité, troisième édition |
|
OMS |
Organisation mondiale de la Santé |
|
PON |
Procédure opératoire normalisée |
|
PSA |
Plan de surveillance administrative |
|
RAPHT |
Règlement sur les agents pathogènes humains et les toxines |
|
RSA |
Règlement sur la santé des animaux |
|
TI |
Technologies de l’information |
Chapitre 1 - Introduction
Les mots soulignés en pointillés sont définis dans le disponible sur le Portail de formation de l’ASPC.
La dans la recherche en sciences de la vie fait référence aux qualités d'un ou d'une , d'une méthode scientifique, d'une propriété intellectuelle ou d'une autre connexe qui leur permettent d'être utilisés autant pour mener des activités scientifiques légitimes que d'être volontairement mal utilisés pour causer du tort ou une . La possibilité que des ressources relatives à la recherche en sciences de la vie soient mal utilisées par des peut entraîner d'importantes préoccupations sociétales, juridiques, éthiques, économiques, de sécurité et de sûretéNote de bas de page1.
Dans le cadre de la recherche en sciences de la vie, il est important de trouver un équilibre entre :
- la progression de la recherche et des technologies dans le domaine des sciences de la vie au profit de la société (p. ex. pour améliorer la santé publique, aider l'environnement, promouvoir la croissance économique);
- la protection de la et de l'environnement contre les possibles associés à certains aspects de la recherche en sciences de la vie qui pourraient être exploités pour causer du tortNote de bas de page2
1.1 Portée
La ligne directrice Gestion des risques associés à la possibilité de double usage dans la recherche en sciences de la vie fournit des conseils détaillés sur la manière d'identifier, d'évaluer et d'atténuer les risques associés à la possibilité de double usage dans la recherche en sciences de la vie impliquant des , et vise à accroître la sensibilisation à ce sujet. Elle vise à faciliter l'évaluation des activités de recherche impliquant des matières biologiques afin de déterminer la probabilité qu'une activité ou ses produits puissent être mal utilisés pour causer du tort, et à fournir des stratégies pour atténuer les risques identifiés. La présente ligne directrice vise également à promouvoir la conduite éthique et responsable de la recherche auprès des scientifiques, des éducateurs, de la , des (ASB), des organismes de financement et des décideurs politiques.
Les renseignements fournis dans le présent document sont présentés à titre indicatif seulement et ne doivent pas être interprétés comme des exigences. Les parties réglementées peuvent choisir d’adopter d’autres approches pour satisfaire aux exigences énoncées dans la Norme canadienne sur la biosécurité, troisième édition (NCB).
1.2 Comment utiliser la ligne directrice Gestion des risques associés à la possibilité de double usage dans la recherche en sciences de la vie
Une liste détaillée de toutes les abréviations et de tous les sigles utilisés dans la présente ligne directrice se trouve au début du document. Chaque mot ou terme est écrit au long à sa première utilisation, suivi de l'abréviation ou du sigle entre parenthèses. Après avoir été définie, l'abréviation est utilisée exclusivement dans le reste du document. Un complet des définitions des termes techniques est disponible sur le Portail de formation de l’ASPC. Les termes définis dans le glossaire sont soulignés en pointillés à leur première utilisation dans la ligne directrice. Lorsqu’une recommandation est associée à une exigence donnée de la NCB, la ou les matrices d’exigences sont citées en référence (p. ex. la matrice 4.1 de la NCB). Une liste complète de références et d’autres ressources est fournie au chapitre 5. Sauf indication contraire, toutes les occurrences du terme « recherche » dans la présente ligne directrice se rapportent spécifiquement à la « recherche en sciences de la vie impliquant des matières biologiques ».
Retour en hautChapitre 2 - Possibilité de double usage
Dans le passé, la possibilité de double usage a eu des conséquences néfastes pour la santé et la sécurité publiques, la population animale, l'environnement et la sécurité nationale. Puisqu’il s’agit toujours d’une préoccupation mondiale, il est essentiel que les gouvernements et les autorités du monde entier insistent sur la nécessité d'une surveillance formelle de la possibilité de double usageNote de bas de page1.
2.1 Histoire
La possibilité de double usage dans la recherche en sciences de la vie a notamment été portée à l'attention du grand public en 2001, après que des lettres contenant des spores de Bacillus anthracis (l'agent causal de l'anthrax) aient été envoyées à deux sénateurs américains et à plusieurs bureaux de médias d’information, entraînant la mort de cinq personnes et l'infection de 17 autresNote de bas de page3. Une enquête ultérieure a révélé que les spores provenaient d'un centre fédéral américain de biodéfense et que la personne accusée d'avoir envoyé les lettres était un scientifique qui avait accès à la bactérie et possédait les compétences et les connaissances nécessaires pour produire les sporesNote de bas de page3,Note de bas de page4. À la suite de cet événement, d'autres cas ont mis en lumière les préoccupations relatives à la possibilité de double usage dans des domaines tels que les maladies infectieuses, les cellules souches, la , la modification génétique des organismes, la génomique et la biologie de synthèseNote de bas de page5,Note de bas de page6. Depuis la pandémie de COVID-19, l'atténuation des risques en matière de et de suscite un intérêt accru dans le monde entier. Actuellement, il existe une grande préoccupation internationale concernant les activités et les renseignements qui pourraient mener au intentionnel ou non d'agents pathogènes à potentiel pandémique, lesquels pourraient avoir des répercussions importantes sur la santé des humains et des animaux dans le monde.
Le tableau 2-1 présente des exemples d'activités de recherche qui ont retenu l'attention à l’échelle internationale en ce qui concerne la possibilité de double usage d'agents pathogènes, de toxines, de connaissances, de techniques ou de technologies. Bon nombre de ces exemples impliquent de la recherche sur le gain de fonction, laquelle comprend la modification d'agents biologiques en vue d'obtenir de nouvelles caractéristiques ou des aptitudes améliorées, souvent en augmentant leur capacité à se reproduire et/ou à infecter des hôtes. L'objectif de la recherche sur le gain de fonction est généralement d'améliorer la compréhension des processus biologiques fondamentaux, tels que la propagation des virus, leur interaction avec les organismes hôtes et leur évolution. Elle peut également aider les chercheurs à anticiper les voies d'évolution possibles afin qu'ils puissent élaborer des contre-mesures, telles que des vaccins ou des traitements, en réponse aux maladies infectieuses émergentes. Cependant, elle peut soulever des préoccupations éthiques et de sécurité, en particulier si les organismes modifiés peuvent présenter des risques accrus pour la santé publique ou l'environnementNote de bas de page7.
|
Activité de recherche |
Possibilité de double usage |
|---|---|
|
2002 - Un poliovirus infectieux a été synthétisé de novo à partir de la structure et de la séquence nucléotidique publiées du génome du poliovirus. |
Bénéfice escompté Démontrer que les virus peuvent être synthétisés de novo (c.-à-d. en l'absence de matrice). Préoccupation relative au mésusage Les méthodes publiées pourraient être utilisées pour la synthèse de novo d'autres virus en utilisant des renseignements génomiques accessibles au public. |
|
2002 - Une protéine du virus de la variole a été synthétisée en utilisant la séquence d'une protéine homologue du virus de la vaccine. La protéine modifiée a été identifiée comme ayant le potentiel d'augmenter la virulence du virus de la vaccine. |
Bénéfice escompté Étudier le rôle prédit de la protéine en tant que facteur de virulence. Préoccupation relative au mésusage Les renseignements issus de la recherche pourraient être utilisés pour élaborer une souche plus pathogène du virus de la vaccine (p. ex. avec une virulence accrue). Cette recherche démontre qu'il est possible de synthétiser les facteurs de virulence du virus de la variole à partir d’agents pathogènes de risque plus faible appartenant à la même famille. |
|
2005 - Le virus de la grippe A(H1N1) responsable de la pandémie de grippe espagnole de 1918 a été reconstitué à l'aide d'un système de génétique inverse.
|
Bénéfice escompté Évaluer les interventions de santé publique actuelles et futures et comprendre la virulence du virus de la grippe. Préoccupation relative au mésusage Le virus reconstitué pourrait être utilisé pour causer du tort (p. ex. par le rejet volontaire, la transformation en arme). Les méthodes publiées pourraient être mal utilisées pour modifier la gamme d'hôtes du virus de l'oiseau à l'humain. |
|
2011 - Une souche du virus de la grippe aviaire A(H5N1) a été modifiée pour étudier et améliorer la transmissibilité par voie aérienne chez les mammifères. |
Bénéfice escompté Étudier la transmission et le développement de souches pathogènes du virus de la grippe aviaire A(H5N1) chez les mammifères afin de déterminer le potentiel pandémique du virus. Préoccupation relative au mésusage La souche virale modifiée présente une transmissibilité accrue et pourrait être utilisée pour causer du tort (p. ex. par le rejet volontaire, la transformation en arme). Le manuscrit publié fournit des renseignements sur les mutations génétiques qui pourraient permettre au virus de devenir plus transmissible chez les mammifères. |
|
2018 - Le virus de la variole équine, un agent pathogène précédemment éteint, a été synthétisé de novo à l'aide d'une séquence génétique accessible au public et de techniques courantes de biologie moléculaire. |
Bénéfice escompté Étudier la possibilité d'utiliser un virus chimérique de la variole équine comme vaccin vivant contre la variole. Préoccupation relative au mésusage Les méthodes publiées pourraient être utilisées pour synthétiser d'autres poxvirus, y compris le virus éradiqué de la variole. |
|
2019 - Le virus Ebola a été généré de novo en utilisant des séquences de virus Ebola fournies par des organisations de la République démocratique du Congo et un système de génétique inverse.
|
Bénéfice escompté Étudier l'efficacité de thérapies expérimentales et de tests diagnostiques contre la souche responsable de l'épidémie de virus Ebola qui a débuté en 2018. Mieux comprendre la relation entre les souches responsables des épidémies de la maladie Ebola. Préoccupation relative au mésusage Les méthodes publiées pourraient être utilisées pour synthétiser les souches associées aux épidémies. |
|
2021 - Des variants du virus SRAS-CoV-2 (l'agent pathogène causal de la COVID-19) ont été créés à l'aide d'un système de génétique inverse.
|
Bénéfice escompté Contribuer à faire progresser la recherche et l'intervention au niveau mondial face à la pandémie de COVID-19. Préoccupation relative au mésusage Les méthodes publiées pourraient être adaptées pour élaborer un variant qui échappe aux traitements et à l'immunité. |
2.2 Surveillance
Au moyen de divers mécanismes législatifs, la surveillance de la possibilité de double usage associée aux agents pathogènes, aux toxines et aux biens et technologies connexes est partagée par plusieurs agences et ministères fédéraux au Canada, notamment :
- l’Agence de la santé publique du Canada (ASPC)
- l’Agence canadienne d'inspection des aliments (ACIA)
- Transports Canada (TC)
- Affaires mondiales Canada (AMC)
- Sécurité publique Canada (SP)
- Innovation, Sciences et Développement économique Canada (ISDE)
- l’Agence des services frontaliers du Canada (ASFC)
- la Gendarmerie royale du Canada (GRC)
Des exemples d'initiatives internationales visant à identifier et à atténuer les risques associés à la possibilité de double usage ainsi que des renseignements sur la situation mondiale actuelle relative à la possibilité de double usage figurent à l'Annexe A.
2.2.1 Législation et réglementation concernant les agents pathogènes et les toxines au Canada
Un est exigé pour effectuer des avec des agents pathogènes humains et des toxines, sauf si une exclusion de la Loi sur les agents pathogènes humains et les toxines (LAPHT) ou une exemption de l'exigence relative à la délivrance de s’appliqueNote de bas de page17,Note de bas de page18. Même lorsqu'elles sont exemptées de l'exigence d’obtenir un permis en vertu de la LAPHT, toutes les personnes menant sciemment des activités réglementées avec un agent pathogène humain ou une toxine sont tenues de prendre toutes les précautions raisonnables pour que celles-ci ne portent atteinte ni à la santé ni à la sécurité publiques [LAPHT 6]Note de bas de page17.
Un ou un est exigé pour l' importation ou le transfert ultérieur ou d'une partie de ceux-ci (p. ex. une toxine), ou d'animaux, de produits ou de sous-produits animaux (p. ex. des tissus, du sérum), ou d'autres organismes porteurs d'un agent pathogène d'animaux terrestres ou d'une partie de celui-ci (p. ex. une toxine) en vertu de la Loi sur la santé des animaux (LSA) et du Règlement sur la santé des animaux (RSA)Note de bas de page19,Note de bas de page20.
Il est de la responsabilité des titulaires de permis de comprendre leurs obligations en vertu de la LAPHT, du Règlement sur les agents pathogènes humains et les toxines (RAPHT), de la LSA et du RSA. En tant que condition de leur permis, les au Canada où sont des doivent satisfaire aux , aux et aux applicables spécifiées dans la NCBNote de bas de page21.
2.2.2 Exportation du Canada
La Loi sur les licences d'exportation et d'importation (LLEI) met en œuvre les contrôles à l' exportation par le biais de la Liste des marchandises et technologies d'exportation contrôlée (LMTEC) du Canada. Cette loi est administrée par AMC et appliquée par l'ASFC et la GRCNote de bas de page22,Note de bas de page23. La LMTEC comprend deux listes qui sont pertinentes dans le contexte de la présente ligne directriceNote de bas de page24 :
- la Liste des marchandises à double usage (marchandises et technologies), qui respecte les engagements pris par le Canada dans le cadre de l'Arrangement de Wassenaar
- la Liste de non-prolifération des armes chimiques et biologiques, qui respecte les engagements du Canada en tant que membre du Groupe d'Australie
De plus amples renseignements sur ces deux listes et sur les licences d'exportation en vertu de la LLEI sont disponibles sur le site Web d'Affaires mondiales Canada.
Retour en hautChapitre 3 - Processus de gestion des risques
Au Canada, une approche fondée sur les risques est utilisée pour appuyer la recherche responsable avec des matières biologiques. La gestion des risques associés à la possibilité de double usage prend en considération le degré de possibilité de double usage (c.-à-d. élevé ou faible), les associés qui sont présents, la probabilité et la gravité d'un événement indésirable et les mesures d'atténuation qui peuvent être mises en œuvre. Un programme de gestion des risques efficace vise à protéger les membres du personnel, la communauté et l'environnement contre l' à des agents pathogènes et à des toxines ou leur rejet. Il vise également à protéger les ressources telles que le matériel de recherche (y compris les agents pathogènes et les toxines), les animaux, l’équipement, les outils, les procédures et les renseignements contre tout mésusage.
Une gestion des risques efficace est appuyée en partie par le respect des obligations législatives fédérales et provinciales ou territoriales applicables, ainsi que des conditions de permis, y compris les exigences applicables de la NCB.
Un Plan de surveillance administrative (PSA) à l’égard des agents pathogènes et des toxines dans un contexte de recherche est un élément clé d'un programme de gestion des risques efficace. Un PSA est exigé pour les demandeurs qui entendent effectuer de la avec des agents pathogènes humains et des toxines [RAPHT 3]. Le PSA définit les mesures administratives, y compris les structures et les systèmes de responsabilisation internes (p. ex. les politiques, les procédures), pour la gestion et le contrôle des risques associés à la biosécurité et la biosûreté dans la recherche en sciences de la vie, y compris ceux associés à la possibilité de double usageNote de bas de page25,Note de bas de page26. Les demandeurs doivent décrire les méthodes et les mécanismes utilisés au sein de l'organisation pour identifier, évaluer et atténuer les risques de double usage tout au long du cycle de vie de la recherche.
La possibilité de double usage est évaluée en déterminant si les ressources issues de la recherche en sciences de la vie pourraient être mal utilisées pour causer du tort ou une maladie. La figure 3-1 peut être utilisée pour guider l'évaluation de la possibilité de double usage, qui peut être élevée ou faible. Il est important de tenir compte du fait que des changements dans les plans de recherche ou des résultats inattendus peuvent affecter le degré de possibilité de double usage associé à un projet particulier. Il est donc important de réévaluer périodiquement le degré de possibilité de double usage, même s'il est initialement considéré comme faible.
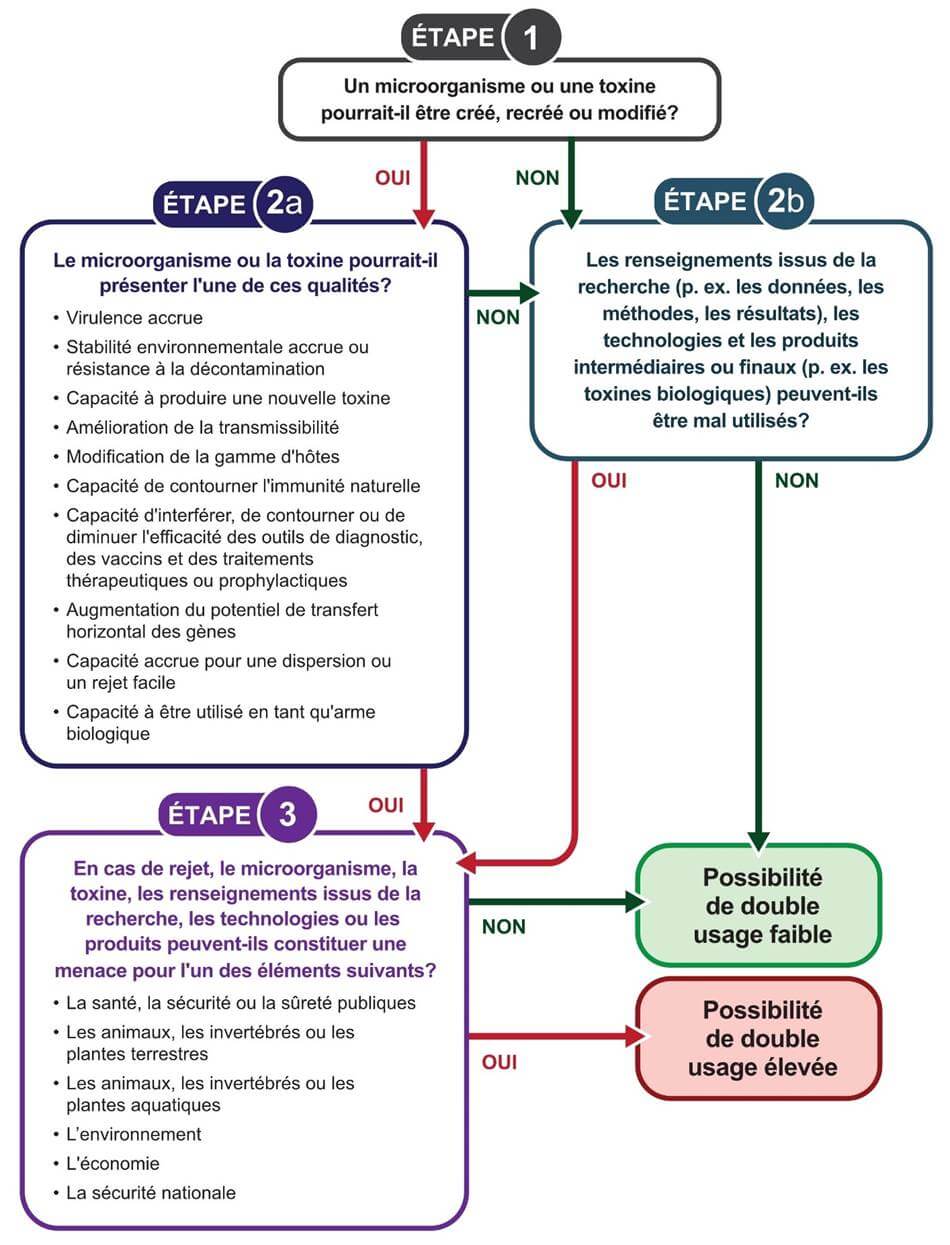
3.1 Identification des dangers
La première étape de la gestion des risques associés à la possibilité de double usage consiste à identifier les dangers. Les dangers sont des sources possibles de dommage, de tort ou d'effets indésirables. Ceux qui présentent une possibilité de double usage comprennent les ressources tangibles et intangibles qui sont utilisées pour des applications scientifiques légitimes, mais qui peuvent aussi être volontairement mal utilisées pour causer du tort ou une maladie chez l’humain, la population animale ou à l'environnement. La Liste de technologies sensibles du Canada décrit les domaines technologiques qui pourraient avoir des répercussions sur la sécurité nationale en cas de mésusage et qui sont donc considérés comme sensibles par le gouvernement du CanadaNote de bas de page27. Les activités sont également prises en compte dans le cadre de cette étape. Il est important de noter que les dangers peuvent influencer les risques associés à d'autres dangers. Par exemple, deux ou plusieurs dangers peuvent être associés individuellement à un risque faible, mais leur combinaison peut présenter un risque moyen ou élevé.
3.1.1 Ressources tangibles
Les ressources tangibles ont des composantes physiques. Des exemples de ressources tangibles qui sont associées à une possibilité de double usage comprennent des matières biologiques, de l’équipement, des outils et des animaux.
3.1.1.1 Matières biologiques
La possibilité de double usage dans la recherche en sciences de la vie est influencée par les caractéristiques inhérentes des agents pathogènes et des toxines utilisés. Par exemple, certains agents pathogènes humains de 3 (GR3) et GR4 et certaines toxines réglementées qui ont une ou une toxicité élevée présentent un risque accru en matière de biosûreté parce qu'ils pourraient être utilisés comme arme biologique contre le grand public. Ceux-ci sont appelés « » (ABCSE). De même, certains agents pathogènes d'animaux terrestres (p. ex. les agents pathogènes d’animaux terrestres désignés par l’ACIA [APAT-DA; comprennent les , les et les relevant de la compétence de l’ACIA]) sont associés à une possibilité de double usage élevée parce qu'ils pourraient être utilisés comme arme biologique agricole. Ce type d'arme biologique pourrait avoir des conséquences négatives sur l'approvisionnement alimentaire national et, par conséquent, sur le commerce et l'économie.
Les risques en matière de biosûreté et la possibilité de double usage peuvent également être accrus avec :
- un agent pathogène qui a été éradiqué ou qui est éteint
- un agent pathogène ou une toxine qui est nouveau (c.-à-d. qui n'a pas été identifié auparavant)
- un agent pathogène ou une toxine qui n'existe pas naturellement dans l'environnement (c.-à-d. qui a été créé ou modifié en )
Il existe également une possibilité de double usage pour les matières biologiques qui ne sont pas réglementées (p. ex. les de GR1, les séquences d'acides nucléiques), car leur manipulation pourrait résulter en la production volontaire ou involontaire d'un agent pathogène réglementé (c.-à-d. GR2 ou plus).
3.1.1.2 Autres ressources tangibles
D'autres ressources tangibles (p. ex. de l’équipement, des outils, des animaux) sont importantes à prendre en compte lors de l'identification des dangers associés à la possibilité de double usage. Par exemple :
- L’équipement et les outils utilisés pour la recherche agricole pourraient être mal utilisés pour disperser des .
- Les technologies émergentes fondées sur l'intelligence artificielle (IA) (p. ex. les plateformes de synthèse robotiques, les dispositifs de criblage à haut débit) pourraient être mal utilisées pour faciliter la production ou la modification rapide de matières biologiques associées à une possibilité de double usage.
- Les animaux infectés par des agents pathogènes à des fins de recherche pourraient être intentionnellement relâchés pour causer du tort à d'autres animaux, à l'humain ou à l'environnement.
3.1.2 Ressources intangibles
Les ressources intangibles n'ont pas de substance physique. Celles qui sont associées à une possibilité de double usage comprennent les renseignements et les connaissances. Des exemples de ressources intangibles comprennent :
- des séquences d'acides nucléiques d'agents pathogènes nouveaux, émergents ou à risque élevé (p. ex. les ABCSE)
- des séquences d'acides nucléiques de gènes de virulence
- des précisions sur des technologies de dissémination d’agents pathogènes ou de toxines (p. ex. l’aérosolisation)
- des instructions relatives aux techniques ou technologies de laboratoire
-
des éléments clés du
d'une organisation (p. ex. le
, le plan de biosûreté), y compris :
- des instructions d'accès à l'installation (p. ex. relatives aux clés, aux cartes d'accès, aux codes d'accès)
- des renseignements concernant la conception et les spécifications techniques de l’installation (p. ex. les points d'entrée, les )
Lors de l'identification de ressources intangibles en tant que dangers associés à une possibilité de double usage, il est important de se demander si les renseignements générés (p. ex. les données, les méthodes) pourraient être utilisés pour menacer la santé, la sécurité ou la sûreté publiques, la santé animale ou l'environnement. Par exemple, les renseignements pourraient être appliqués à des matières biologiques de risque plus élevé, ou ils pourraient être utilisés pour mettre en évidence une dans la surveillance des agents pathogènes, la capacité de santé publique ou la préparation en matière de sécurité publique.
Les ressources intangibles pourraient faire l'objet d'une mauvaise application ou d’un mésusage à des fins malveillantes. Voici quelques exemples de mauvaise application ou de mésusage :
- Des renseignements issus de la recherche sur le développement de microorganismes résistants aux médicaments, destinés à améliorer la compréhension des traitements et des mécanismes de résistance, pourraient être utilisés pour élaborer des organismes capables d'échapper aux traitements disponibles.
- Une méthode utilisée pour la dispersion d'un biopesticide de GR1 sur des cultures pourrait être utilisée pour la dispersion d'une arme biologique aérosolisée.
- Des renseignements issus de la recherche sur des microorganismes à faible risque pourraient être appliqués à des agents pathogènes à risque élevé apparentés (p. ex. entre les poxvirus).
- Des algorithmes d'IA pourraient faire l’objet de mésusage pour créer des armes biologiquesNote de bas de page28. Par exemple, les algorithmes d'IA avancés en matière d'analyse génomique peuvent rapidement identifier des facteurs de virulence et prédire les interactions entre l'agent pathogène et l'hôte. Bien que ces algorithmes puissent améliorer notre compréhension des agents pathogènes, ils pourraient aussi être modifiés pour concevoir des toxines ou produire des agents pathogènes sur mesure.
3.1.3 Activités
Qu'une activité de recherche implique une matière réglementée ou d'autres matières biologiques, la possibilité de double usage peut être influencée par les aspects inhérents aux méthodes de recherche. Certaines techniques et méthodes sont plus susceptibles d'être mal utilisées, même si l'objectif de la recherche était bien intentionné. Voici quelques exemples de techniques et de méthodes qui pourraient présenter une possibilité de double usage :
- La recherche impliquant le passage d'un agent pathogène dans un hôte animal peut être utilisée pour étudier l'évolution d'un agent pathogène ou pour développer des vaccins. Toutefois, ces méthodes pourraient également être utilisées pour sélectionner une souche d'agent pathogène présentant une infectiosité, une et une transmissibilité accrues chez l'humain et l'animal.
- Des techniques de biologie moléculaire de routine peuvent être utilisées pour la synthèse de novo d'un microorganisme non pathogène (p. ex. en utilisant des oligonucléotides achetés auprès d'une source commerciale, en utilisant des séquences d'acides nucléiques publiées pour la synthèse). Ces mêmes techniques peuvent également être utilisées pour la synthèse de novo d'un agent pathogène qu'il serait autrement difficile d'acquérir.
- Les techniques de passage en série et d'édition de gènes sont souvent associées à une faible possibilité de double usage (p. ex. lorsqu'elles sont utilisées pour créer des modèles à gène invalidé [knock-out] afin d'étudier la régulation des gènes bactériens). Toutefois, ces techniques pourraient également être appliquées à de la recherche sur le gain de fonction à possibilité de double usage élevée, ce qui pourrait susciter des préoccupations liées à la santé publique, à la santé animale ou à l'environnementNote de bas de page29. La recherche sur le gain de fonction vise à modifier des agents biologiques pour créer de nouvelles caractéristiques ou améliorer leurs aptitudes, souvent en augmentant leur capacité à se répliquer et/ou à infecter des hôtes (p. ex. en insérant un facteur de virulence dans le génome d'un microorganisme hôte pour développer un agent pathogène nouveau ou modifié).
- La manipulation épigénétique pourrait possiblement être utilisée pour traiter des maladies en modifiant les profils d'expression des gènes afin d'améliorer l'efficacité des immunothérapiesNote de bas de page30. Cependant, elle pourrait également être mal utilisée pour altérer la réponse immunitaire d’un hôte ou augmenter la pathogénicitéNote de bas de page31.
- L'IA peut être utilisée pour optimiser les modèles des plateformes de diagnostic. Toutefois, l'IA pourrait également être mal utilisée pour altérer des résultats de diagnostic.
Bien que toutes les recherches portant sur un agent pathogène ou une toxine présentent un certain degré de possibilité de double usage, les activités de recherche comme les suivantes peuvent contribuer à la possibilité de double usage d'un projet :
- la création d'un nouvel agent pathogène
- la création de nouveaux produits intermédiaires ou finaux (p. ex. des toxines)
- la réalisation d'activités avec un agent pathogène ou une toxine nouveaux ou émergents
- la reconstitution d'un agent pathogène existant, disparu ou éradiqué (p. ex. la synthèse de novo)
- l’utilisation, l’élaboration ou l’amélioration de techniques ou de technologies nouvelles ou émergentes pour la dissémination d'agents pathogènes ou de toxines (p. ex. de nouvelles technologies d'aérosolisation)
- la modification d'un agent pathogène ou d'une toxine (p. ex. l’augmentation de la résistance aux médicaments, de l'évasion immunitaire, de la pathogénicité ou de la virulence d'une bactérie)
La modification d'un agent pathogène ou d'une toxine peut entraîner une classification dans un groupe de risque plus élevé et peut introduire d'autres dangers. Un examen de la littérature scientifique existante peut aider à déterminer si des résultats inattendus ont été observés dans des études similaires (p. ex. avec des agents pathogènes apparentés). Des renseignements de substitution provenant d'agents pathogènes génétiquement apparentés peuvent être utilisés pour évaluer les risques associés à de nouveaux agents pathogènes dont la pathogénicité est inconnue. De même, pour les nouvelles toxines dont la toxicité est inconnue, des renseignements de substitution provenant d'une toxine structurellement similaire peuvent être utilisésNote de bas de page32,Note de bas de page33,Note de bas de page34. Même en l'absence de tels renseignements, les activités prévues peuvent être évaluées en fonction de la possibilité qu’elles produisent des résultats inattendus. Le produit des activités peut faire l'objet d'une pour déterminer la possibilité qu’il soit classé dans un groupe de risque plus élevé. Des renseignements supplémentaires sont disponibles dans la Ligne directrice canadienne sur la biosécurité – Évaluation des risques associés à l'agent pathogèneNote de bas de page35.
3.2 Évaluation des risques
Les risques associés à la possibilité de double usage sont déterminés en tenant compte de la probabilité qu'un événement indésirable se produise et de la gravité de ses conséquences. Une matrice d'évaluation des risques, telle que celle de la figure 3-2, peut aider à évaluer le niveau de chaque risque associé à la possibilité de double usage d'un projet de recherche. Même si le risque global associé à la possibilité de double usage est initialement jugé faible, il demeure important de surveiller l'évolution de la situation au fur et à mesure que la recherche progresse.
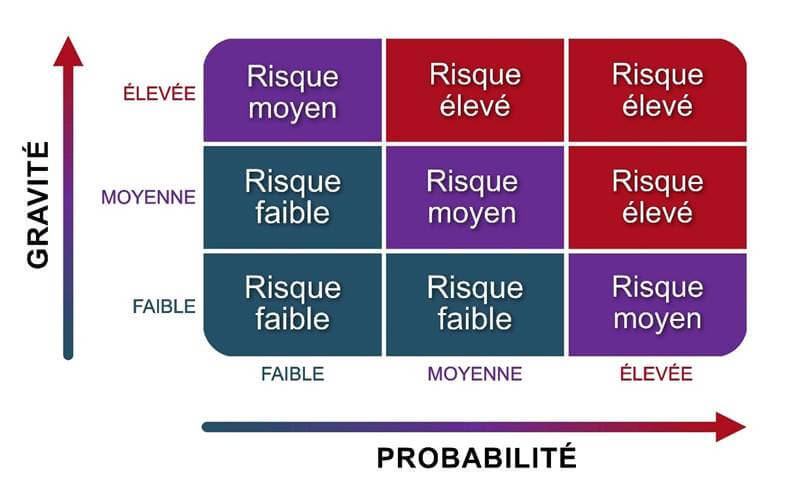
3.2.1 Évaluation de la probabilité
Une évaluation de la probabilité prend en compte la probabilité qu'un événement se produise. Pour aider à déterminer la probabilité qu'un événement se produise, il est important de prendre en compte les facteurs liés au motif, aux moyens et à la capacité de mésusage intentionnel des agents pathogènes, des toxines, des renseignements ou des technologies, y compris les suivants :
Conditions de laboratoire
- Quelles sont les conditions de laboratoire nécessaires pour répéter l'expérience ou la reproduire à plus grande échelle?
- Serait-il possible de mener les travaux en dehors d'un laboratoire entièrement équipé?
- Les conditions de laboratoire nécessaires sont-elles difficiles à réunir ou peuvent-elles être facilement reproduites dans un laboratoire improvisé?
- Les technologies de laboratoire sur puce ou les systèmes d'automatisation de laboratoire basés sur l'IA pourraient-ils faciliter l'expérimentation en optimisant les conditions, en améliorant l'extensibilité ou en réduisant la dépendance envers des laboratoires entièrement équipés?
Compétences techniques
- Quelles sont les compétences techniques nécessaires pour répéter l'expérience ou la reproduire à plus grande échelle?
- Le travail pourrait-il être reproduit à l'aide de l'IA ou par une personne ayant peu de formation scientifique ou de compétences techniques (p. ex. des plateformes de synthèse automatisées fondées sur l'IA réduisant le besoin d'expertise spécialisée)?
Acquisition de ressources
- Le matériel, les outils et l’équipement nécessaires à la réalisation de l'expérience sont-ils coûteux ou hautement spécialisés?
- Les ressources, les outils et l’équipement sont-ils réglementés (p. ex. l’équipement figurant sur les listes de contrôle à l’exportation du Groupe d'Australie) ou disponibles à l’achat pour le grand public?
- Des composants spécialisés pourraient-ils être imprimés en 3D?
- Les activités de recherche pourraient-elles être sous-traitées sous de faux prétextes?
Application à des organismes à risque plus élevé
- Les renseignements ou les techniques associées à des organismes à plus faible risque (p. ex. le virus de la variole équine) peuvent-ils être facilement appliqués à des organismes à risque plus élevé (p. ex. le virus de la variole)?
Cadre temporel
- Le délai de production des agents pathogènes ou des toxines pourrait-il être raccourci (p. ex. grâce à l'accès à de l’équipement biotechnologique à grande échelle ou à des technologies d'IA)?
- La ressource (p. ex. un agent pathogène, une toxine, des résultats de recherche, des renseignements, une technique) pourrait-elle être mal utilisée dans son état actuel, ou des améliorations sont-elles nécessaires avant qu'elle ne puisse être utilisée pour causer du tort?
Historique de l'événement
- Un mésusage impliquant la ressource ou une ressource similaire (p. ex. un agent pathogène, une toxine, des renseignements, une technique) s'est-il déjà produit au sein de l'organisation, de la région, du pays ou ailleurs dans le monde? Si oui, à quelle fréquence cela s'est-il produit?
Motif
- Dans quelle mesure un adversaire pourrait-il être intéressé ou motivé par l'obtention de l'agent pathogène, de la toxine, des renseignements ou de la technologie à des fins malveillantes? Les adversaires peuvent comprendre des membres du personnel, des entrepreneurs, des investisseurs étrangers, des partenaires de recherche ou des activistes qui n'ont pas le .
- Existe-t-il des preuves que la recherche pourrait intéresser des adversaires (p. ex. des rapports ou des déclarations émanant de sources de renseignement telles que le Service canadien du renseignement de sécurité et le Centre de la sécurité des télécommunications Canada, des déclarations relatives à la sécurité de la recherche émanant du gouvernement du Canada)Note de bas de page36,Note de bas de page37?
3.2.2 Évaluation de la gravité
Lors de l'évaluation de la gravité des conséquences possibles liées au rejet ou au mésusage d'un agent pathogène, d'une toxine, d'une technologie ou de renseignements, il est important de tenir compte des répercussions sur les aspects suivants :
Santé humaine et animale
- Quelle quantité d'agent pathogène ou de toxine cause une infection, une maladie ou une ?
- Quel est le degré de transmissibilité de l'agent pathogène entre les espèces et au sein de celles-ci (p. ex. l'humain, les animaux)?
- Quelle est la gravité de l'infection, de la maladie ou de l'intoxication associée à l'agent pathogène ou à la toxine (p. ex. entraîne-t-elle une maladie grave ou la mort)?
- Quel serait l'impact de la recherche sur les mesures de prévention des infections, la prise en charge et le traitement médical, la surveillance et la détection des maladies ou le d'un agent pathogène au niveau régional, national ou mondial?
- Des vaccins efficaces ou des traitements prophylactiques et post-exposition sont-ils disponibles pour réduire la gravité ou la transmission de l'infection, de la maladie ou de l'intoxication?
Environnement
- L'agent pathogène peut-il survivre, persister, se disperser ou proliférer dans l'environnement?
- L'agent pathogène ou la toxine peuvent-ils altérer les écosystèmes, déplacer des espèces, avoir un impact négatif sur des cultures importantes pour l'agriculture ou nuire à la biodiversité?
Perception du public
- Les risques associés à la recherche scientifique sont-ils facilement compris par le grand public, les médias ou d'autres personnes sans formation scientifique?
- La recherche pourrait-elle faire l'objet de mésinformation?
Sécurité nationale et économie
- Comment une infection, une maladie ou une intoxication généralisée pourrait-elle compromettre les infrastructures critiques ou l'économie (p. ex. l’agriculture, les hôpitaux, l’importation et l’exportation de marchandises)?
3.3 Atténuation des risques
Chacun a la responsabilité d'atténuer les risques associés aux connaissances, aux renseignements, aux méthodes, aux produits ou aux technologies qu'il élabore. L'atténuation des risques est un processus continu dans lequel des mesures spécifiques sont mises en place pour réduire au minimum la probabilité d'un ou la gravité de ses conséquences s'il se produit. Les mesures d'atténuation appropriées dépendent des risques identifiés et peuvent être de nature physique ou opérationnelle. Par exemple, les mesures d'atténuation peuvent comprendre la mise en œuvre de codes de conduite, le filtrage du personnel, des barrières de sécurité physiques ou logiques, la gestion des , la destruction ou la des matières, des mesures de cybersécurité et des mesures d'urgence ou de prévention des incidents.
Une fois les mesures d'atténuation des risques mises en œuvre, elles font l’objet d’une surveillance par l'autorité appropriée (p. ex. les membres du personnel de laboratoire, le chercheur principal, l'ASB, la haute direction, le comité institutionnel de biosécurité [CIB], les autorités réglementaires, d'autres organismes de surveillance). Il est important de noter qu'à moins qu'une activité ne soit pas menée, les risques ne peuvent pas être complètement éliminés, quelle que soit la stratégie d'atténuation.
L'objectif de l'atténuation des risques est de réduire les risques identifiés à un niveau jugé acceptable selon le seuil de tolérance au risque d'une organisation. Le seuil de tolérance au risque est établi par l'organisation et s'aligne sur les politiques internes, lesquelles appuient la conformité à la législation et à la réglementation applicables (p. ex. la LAPHT, le RAPHT, la LSA, le RSA)Note de bas de page38. Les considérations qui peuvent également être prises en compte dans le seuil de tolérance au risque établi comprennent :
- le risque perçu (p. ex. par le grand public)
- le risque d’atteinte à la réputation (p. ex. la perte de crédibilité au sein de la communauté scientifique)
- le risque financier (p. ex. une perte de financement)
L'atténuation des risques peut également être appuyée par la mise en œuvre de normes et de lignes directrices internationales (p. ex. ISO 35001 – Système de management des biorisques pour les laboratoires et autres organismes associés)Note de bas de page39.
3.3.1 Mesures de biosûreté pour les ressources intangibles
Lors de la mise en œuvre de mesures d'atténuation pour protéger contre le mésusage des ressources intangibles, il est important de tenir compte de la manière dont on pourrait y accéder. Par exemple, des adversaires peuvent contourner les mesures de sécurité opérationnelles ou physiques pour accéder aux ressources, les utiliser, les modifier, les divulguer ou les détruire (p. ex. par le biais de cyberattaques, d'un accès non autorisé au réseau de technologies de l’information [TI] ou par la création de brèches dans des barrières physiques).
Les mesures d'atténuation visant à empêcher l'accès aux ressources intangibles par des adversaires peuvent comprendre :
- des contrôles de sécurité, tels qu'un filtrage de sécurité plus strict des membres du personnel ou des mesures de sécurité physique accrues dans les locaux d'une installation où sont conservés des
- des (PON) pour aider à sécuriser les ressources lorsqu'elles ne sont pas utilisées
- une formation sur les ressources intangibles afin d'aider les membres du personnel à reconnaître les renseignements sensibles qu'ils ont en leur possession et les mesures de sécurité nécessaires pour les protéger
Les membres du personnel peuvent avoir accès à des ressources intangibles (p. ex. des renseignements, des connaissances) lorsqu'ils participent directement ou indirectement à un projet de recherche. Des programmes de formation robustes sur les ressources intangibles couvrent l'importance d'une politique en matière de rangement du bureau, de l’entreposage des renseignements sensibles dans des emplacements sécurisés, de la gestion des clés et des cartes d'accès, et du respect des PON pour sécuriser les renseignements sur le réseau TI de l'organisation, les disques durs, les dispositifs de stockage externes et d'autres emplacements de stockage de documents électroniques. Le programme de formation peut également promouvoir des pratiques qui atténuent les risques de cyberattaques, telles que les escroqueries par hameçonnage et les attaques par maliciel. Par exemple, une organisation pourrait former les membres du personnel à utiliser des mots de passe forts pour se connecter à des comptes et à chiffrer les renseignements sensibles avant de les partager avec des collaborateurs. Les séances de formation sur les ressources intangibles peuvent également comprendre le plan de communication d'une organisation pour le partage des renseignements sensibles (p. ex. dans les résumés, les présentations, les affiches), tel que déterminé par le plan de biosûreté. Des renseignements supplémentaires sur les mesures de biosûreté pour le 4 (NC4) sont disponibles dans l'Addenda de biosûreté apporté à la Norme canadienne sur la biosécurité, troisième édition (l'Addenda de biosûreté)Note de bas de page40.
3.3.2 Plan de communication
Un plan de communication est un élément important pour aider à atténuer les risques associés à la possibilité de double usage. En déterminant comment, quand, à qui et quels renseignements peuvent être communiqués, le plan de communication fournit un cadre pour aider à protéger les renseignements sensibles et à communiquer les détails de la recherche de manière responsable.
Public cible
Le plan de communication peut identifier les personnes avec lesquelles les renseignements peuvent être partagés. Le public cible peut comprendre la communauté scientifique, le grand public ou un petit groupe de parties prenantes ou de collaborateurs de confiance.
Calendrier
Le plan de communication peut indiquer quand les membres du personnel peuvent communiquer des résultats ou des renseignements. Par exemple, il peut contenir des considérations et des PON pour les messages réactifs ou proactifs, ainsi que des processus d'examen préalable à la publication ou à la communication qui aident à déterminer le moment stratégique pour diffuser les communications de manière responsable.
Le fait de diffuser de manière proactive des communications avec les médias pour le grand public peut aider à mettre en évidence la valeur de la recherche et les mesures d'atténuation en place pour améliorer la compréhension du public. Cela peut aider à prévenir la propagation de mésinformation (c.-à-d. des faussetés accidentelles partagées sans intention de nuire) et de désinformation (c.-à-d. des faussetés délibérées partagées avec des intentions malveillantes). Il est également important de garder à l'esprit que les plans et les résultats de recherche sont souvent communiqués à de nombreux moments tout au long du processus de recherche, et non seulement après son achèvement. Au-delà de la publication dans une revue scientifique, les renseignements peuvent également être communiqués dans le cadre de :
- la conception du projet
- la demande de financement
- l’approbation institutionnelle
- l’examen de la littérature et du processus expérimental
- l’élaboration de manuscrits ou d'autres moyens de communiquer les résultats de la recherche (p. ex. la prépublication d'un article, une présentation lors d'une conférence, le dépôt d'une demande de brevet).
- la publication de renseignements sur les bases de données de financement accessibles au public
- rapports d’étape relatifs au financement
Moyens de communication
Les renseignements ou les résultats relatifs à la recherche en sciences de la vie peuvent être diffusés par le biais d'articles de revues scientifiques, d'éditoriaux, de communiqués de presse, de présentations orales, de conférences, de communications par courrier électronique chiffré, et plus encore. Le plan de communication peut déterminer quel moyen de communication est approprié en fonction des renseignements à partager.
Contenu
Le plan de communication peut préciser les types de renseignements et le niveau de détail qui peuvent être diffusés, ainsi que les renseignements qui doivent être omis.
La possibilité de double usage et les préoccupations en matière de biosûreté peuvent avoir une incidence sur les renseignements que les scientifiques décident de transmettre dans leurs communications. Si les dommages possibles relatifs à la publication de certains renseignements l'emportent sur les bénéfices possibles, il est important d'envisager de les omettre ou de s'abstenir de publier. Par exemple, des renseignements sensibles, tels que du matériel et des méthodes spécifiques, peuvent être omis dans un manuscrit afin de protéger les renseignements contre des adversaires. Bien que l'omission de certains détails puisse faire partie d'une communication scientifique responsable lorsqu'il s'agit de travaux portant sur des agents pathogènes ou des toxines présentant une possibilité de double usage, des détails suffisants sont néanmoins nécessaires pour appuyer l'intégrité scientifique de la recherche.
La décision d'omettre des renseignements sensibles dans les manuscrits publiés est prise en tenant soigneusement compte de l'équilibre entre le progrès scientifique et la protection des renseignements sensibles contre des adversaires. Le plan de communication peut faciliter la prise de décision concernant le contenu des communications, en identifiant les circonstances qui justifieraient l'omission de renseignements dans un manuscrit.
Lors de la préparation d'un manuscrit pour l'examen par les pairs et la publication, les chercheurs, l'ASB, le CIB et la haute direction peuvent poser des questions telles que les suivantes :
- Comment les renseignements pourraient-ils être mal utilisés s’ils étaient publiés?
- Qui pourrait bénéficier de la recherche et qui pourrait être victime du mésusage de la recherche?
- Le manuscrit contiendra-t-il des renseignements sensibles (p. ex. la séquence génétique d'un facteur de virulence modifié, un processus de modification de la gamme d'hôtes d'un agent pathogène)?
- Certains renseignements sensibles devraient-ils être supprimés avant la soumission?
- Le manuscrit devrait-il comprendre une section décrivant les mesures de biosûreté supplémentaires mises en œuvre pour atténuer la possibilité de double usage du projet de recherche (p. ex. l’examen par un comité de biosûreté)?
- L'éditeur évalue-t-il les manuscrits afin de déterminer s’ils présentent une possibilité de double usage et ses examinateurs pourraient-ils aider à déterminer quels renseignements, le cas échéant, devraient être omis?
De plus, il est recommandé d'avertir les rédacteurs en chef, les examinateurs ou les conseils consultatifs concernés de tout contenu susceptible d'être associé à une possibilité de double usage.
3.3.3 Modifications apportées à la conception expérimentale
Des modifications apportées à la conception expérimentale peuvent permettre une recherche plus sécuritaire sans compromettre les objectifs de la recherche. Les aspects suivants d'un projet de recherche peuvent être modifiés afin de réduire la possibilité de double usage :
Sélection des agents pathogènes
Il est préférable, notamment du point de vue de la possibilité de double usage, de travailler avec une alternative moins pathogène lorsqu'il est possible d'obtenir des résultats comparables. Par exemple, un agent pathogène ayant une large gamme d'environnements et d'hôtes pourrait être :
- remplacé par une souche atténuée qui ne peut pas se développer correctement dans l'environnement à l’extérieur du laboratoire ou chez l'humain
- remplacé par une souche auxotrophe (c.-à-d. incapable de synthétiser une substance nécessaire à sa croissance)
- remplacé par un composant d'un agent pathogène (p. ex. une protéine virale au lieu d'un virus entier)
- inactivé (c.-à-d. rendu totalement non infectieux)
Il est également important de se demander si les objectifs de la recherche peuvent être atteints en utilisant un agent pathogène pour lequel des contre-mesures médicales (c.-à-d. de la prophylaxie, des traitements thérapeutiques) sont disponibles. En général, un risque plus élevé est associé aux agents pathogènes qui provoquent des maladies pour lesquelles il n'y a pas de traitement disponible. Il est donc recommandé de :
- choisir un agent pathogène pour lequel il existe des thérapies prophylactiques ou post-exposition efficaces (p. ex. des vaccins, des médicaments antiviraux)
- tester la sensibilité d'un agent pathogène aux thérapies prophylactiques ou post-exposition s'il n'existe pas de contre-mesures connues
Type de travail
En combinaison avec des mesures de biosûreté appropriées, l'analyse in silico (c.-à-d. des simulations, de la modélisation et de l'analyse de données informatisées) pourrait être utilisée au lieu de mener des expériences in vivo ou . L'analyse in silico permet d'explorer en détail des scénarios complexes et est associée à moins de préoccupations en matière de biosécurité, telles que l'exposition à des agents pathogènes lors d'expériences physiquesNote de bas de page41.
Technique de laboratoire
Les objectifs de la recherche peuvent parfois être atteints en utilisant des techniques de laboratoire de rechange qui ne sont pas associées à un risque d'exposition ou de rejet. Par exemple, des tests de neutralisation d'anticorps pourraient être utilisés au lieu d'exposer des modèles expérimentaux à des agents pathogènes vivants.
3.4 Examen et amélioration continue
Le degré de possibilité de double usage associé à un projet de recherche en sciences de la vie peut évoluer dans le temps en raison de divers facteurs, notamment de nouvelles découvertes expérimentales ou la disponibilité de nouvelles technologies. Il est donc recommandé d'examiner continuellement la possibilité de double usage associée à un projet dans le cadre d'un examen périodique de l' (matrice 4.1 de la NCB). Cet examen continu est essentiel pour identifier et évaluer les risques nouveaux, changeants ou émergents, et pour mettre en œuvre des mesures d'atténuation nouvelles ou améliorées le cas échéant.
La fréquence de l'examen de l'évaluation des risques de biosûreté dépend des risques associés aux ressources et aux activités. L’examen peut être régulier ou déclenché par certains changements (p. ex. en cas de résultats inattendus). Lorsqu'une évaluation des risques de biosûreté est répétée ou examinée, il est important de mettre à jour le plan de biosûreté en conséquence (matrice 4.1 de la NCB). Le plan de biosûreté est adapté à chaque installation et son niveau de détail et de complexité varie en fonction des activités menées. Par exemple, des mesures de sécurité accrues sont nécessaires pour travailler avec des agents pathogènes et des toxines ayant été déterminés comme présentant une possibilité de double usage accrue (p. ex. les ABCSE). Lorsqu'une augmentation de la possibilité de double usage est identifiée, la répétition des évaluations des risques permet de déterminer si de nouvelles mesures d'atténuation sont nécessaires. En fonction de l'évaluation des risques de biosûreté, si les risques sont jugés trop élevés par rapport aux bénéfices escomptés, ou si les mesures d'atténuation des risques ne sont pas réalisables, il peut être nécessaire de modifier le projet, ou de déplacer les expériences dans une installation disposant d'une meilleure capacité d'atténuation des risques. Dans certains cas, il peut s'avérer nécessaire d'arrêter la recherche ou de la mettre en pause jusqu'à ce que des mesures d'atténuation appropriées puissent être mises en œuvre.
Le fait de discuter régulièrement de la possibilité de double usage tout au long d'un projet peut aider à identifier les dangers, à évaluer les risques et à faciliter l'élaboration de mesures d'atténuation des risques appropriées et adaptables. Ces discussions peuvent comprendre des personnes et des groupes ayant une expertise pertinente, tels que :
- le titulaire de permis
- les chercheurs principaux
- les collaborateurs internes ou externes
- les membres du personnel de recherche et de laboratoire
- la haute direction
- l'ASB
- le CIB
- les membres du personnel de sécurité
- des éthiciens
- les organismes de financement
- des experts en communication ou en relations publiques
- des conseillers juridiques
- les ministères gouvernementaux et les organismes de réglementation compétents
- des représentants du grand public
Le CIB est composé de membres ayant des points de vue différents, tels que des membres du personnel de laboratoire, des professionnels de la santé, la haute direction et les ASB. En raison de son rôle dans la gestion du programme de biosécurité et de l'éventail d'expertise, de compétences et de connaissances que lui confère la diversité de ses membres, un CIB constitue une excellente ressource pour effectuer ou appuyer des évaluations des risques sans trop restreindre la recherche. S'ils ont reçu une formation appropriée pour identifier les risques, les membres du personnel de laboratoire et les chercheurs principaux peuvent également être impliqués dans le processus d'évaluation des risques, car ce sont eux qui connaissent le mieux la recherche prévue, les résultats possibles et les contributions.
Les commentaires des représentants du public peuvent donner une idée de la manière dont un projet de recherche est perçu, ce qui peut guider l'élaboration d'un plan de communication visant à répondre aux préoccupations du public lorsque les résultats de la recherche sont publiés. Le fait de ne pas examiner les projets de recherche sous l'angle de la possibilité de double usage avec un large éventail de parties prenantes peut accroître la probabilité de mésusage du matériel ou des renseignements qui en résultent.
Retour en hautChapitre 4 - Opportunités de gestion des risques tout au long d'un projet de recherche
Il est important d'évaluer la possibilité de double usage et de mettre en œuvre des stratégies de gestion des risques tout au long d'un projet de recherche. Ce chapitre explique comment chaque étape d'un projet de recherche offre une opportunité de gestion des risques associés à la possibilité de double usage.
4.1 Évaluation de la capacité et de l’infrastructure
Il est essentiel que les organisations disposent d'une capacité et d'une infrastructure suffisantes pour accueillir la recherche associée à une possibilité de double usage avant le début du projet. Cela comprend des membres du personnel qualifiés, une surveillance interne, une conception physique appropriée, des établies et l'équipement nécessaire pour atténuer les risques associés à la possibilité de double usage. Compte tenu de la numérisation croissante des projets de recherche ainsi que du ciblage accru du secteur de la santé par des adversaires, il est important de disposer d'une infrastructure de cybersécurité adéquate pour sécuriser le projet tout au long de son cycle de vie. Il est donc important que les organisations évaluent si la capacité et l'infrastructure existantes peuvent accueillir de nouvelles activités de recherche et si les mesures d'atténuation en place sont suffisantes.
La formation, le développement et la formation continue contribuent à doter les membres du personnel des connaissances nécessaires pour évaluer les risques, les avantages et les implications sociales plus larges de la recherche en sciences de la vie. La plupart des membres du personnel de recherche recrutés par une organisation possèdent probablement des connaissances de base sur la possibilité de double usage, acquises au cours de leurs études secondaires, de leurs études post-secondaires, de leurs stages ou de concours en science, technologie, ingénierie et mathématiques (STIM). Toutefois, les organisations peuvent proposer aux membres de leur personnel des programmes de formation sur mesure et des opportunités de formation continue afin de renforcer leur compréhension de la possibilité de double usage. Les codes de conduite et les PON peuvent également appuyer la capacité des membres du personnel d'une organisation à atténuer suffisamment les risques associés à la possibilité de double usage. Des comités formés à la gestion des risques et à l'éthique de la recherche peuvent être mis en place pour fournir des conseils et assurer une surveillance administrative.
Compte tenu de la nature multidisciplinaire et parfois convergente de la recherche et de l'innovation scientifiques, il est important d'étendre l'éducation sur la possibilité de double usage aux membres du personnel tels que les ingénieurs, les informaticiens et les spécialistes des sciences sociales. Les activités de sensibilisation dans ces domaines peuvent être structurées par le biais de formations organisationnelles ou dans le cadre de collaborations de recherche, mais elles peuvent également se faire par le biais d'un partage informel des connaissances.
4.2 Planification du projet
La possibilité de double usage peut être évaluée bien avant que la recherche ne soit entamée dans le laboratoire. Le concept et le plan d'ensemble du projet peuvent être évalués afin d'identifier la possibilité de double usage, les mesures d'atténuation appropriées et les modifications à apporter pour réduire les risques.
L'objectif de l'évaluation de la possibilité de double usage au stade de la planification est d'établir un profil de risque et de déterminer si celui-ci se trouve à l’intérieur du cadre de tolérance au risque de l'organisation et est conforme à la législation et à la réglementation applicables. Idéalement, l'évaluation de la possibilité de double usage est effectuée par des personnes ayant des expertises, des perspectives et des responsabilités différentes. Par exemple, bien que les chercheurs soient ceux qui connaissent le mieux leur travail et qu’ils soient bien placés pour évaluer les bénéfices et les dommages possibles associés à leurs projets, leur point de vue peut être biaisé.
Lorsque la recherche scientifique est interdisciplinaire, plusieurs parties prenantes et secteurs travaillent en collaboration pour mener la recherche. Dans ce cas, les scientifiques, les organisations, les organismes de financement, les rédacteurs en chef et les décideurs politiques des secteurs privé ou public peuvent partager la responsabilité de l'atténuation des risques associés à la recherche. L'Organisation mondiale de la Santé (OMS) fournit des listes de vérification à l'intention des différentes parties prenantes tout au long du continuum de recherche afin de les aider à gérer les risques associés à la possibilité de double usageNote de bas de page1.
4.3 Approbation et financement
Avant que la recherche présentant une possibilité de double usage ne soit approuvée, il est important que la proposition de recherche soit examinée par les membres du personnel des organes de l'organisation formés à la gestion des risques (p. ex. le CIB, le comité interne d'examen du financement, le bureau de sécurité de la recherche), la haute direction et l'ASB. Ces personnes peuvent collaborer pour évaluer si les risques associés à la possibilité de double usage sont suffisamment gérés avant que le financement ne soit accordé par l'organisation ou qu'une demande de subvention ne soit soumise aux organismes de financement.
Tout au long du processus d'approbation, il est important d'être au courant de tous les accords en place concernant la possibilité de double usage. Ceux-ci peuvent comprendre des accords avec des organismes externes non réglementaires, tels que des organismes de financement et des éditeurs, ou avec des personnes ou des organismes de surveillance internes, tels que le CIB, l'ASB et les membres du personnel de laboratoire. Les universités et les institutions de recherche affiliées qui dépendent du financement des organismes subventionnaires fédéraux doivent se conformer à la Politique sur la recherche en technologies sensibles et sur les affiliations préoccupantes et aux Lignes directrices sur la sécurité nationale pour les partenariats de recherche du gouvernement du Canada, le cas échéantNote de bas de page42,Note de bas de page43. La politique interdit le financement fédéral de projets visant à faire progresser les domaines de recherche sur les technologies sensibles si l'un des chercheurs impliqués est affilié à, ou reçoit du financement ou une contribution en nature de, certaines organisations de recherche qui pourraient poser un risque pour la sécurité nationale du Canada (c.-à-d. sur la liste des Organisations de recherche nommées)Note de bas de page44,Note de bas de page45. Les lignes directrices aident les chercheurs, les organisations de recherche et les organismes de financement fédéraux à atténuer les risques possibles pour la sécurité nationale qui pourraient être associés aux partenariats de recherche.
Il est important que les organisations qui distribuent des fonds à plusieurs chercheurs élaborent des politiques et des lignes directrices pour régir l'administration des fonds. Des politiques et des lignes directrices peuvent également être élaborées pour indiquer clairement comment identifier et communiquer les risques et les stratégies d'atténuation. Elles éclairent l'examen et l'approbation des propositions de recherche avant qu'elles ne soient soumises à un organisme de financement. Les discussions entre les chercheurs et les administrateurs des organismes de financement peuvent permettre de répondre aux préoccupations et de préciser des éléments de la proposition de recherche, y compris la possibilité de double usage et les stratégies d'atténuation.
4.4 Recherche
Il arrive que la possibilité de double usage ne devienne évidente qu'au fur et à mesure de l'avancement d'un examen approfondi de la littérature ou lorsque des résultats sont générés. Il est donc recommandé de réévaluer le profil de risque et les mesures d'atténuation existantes lorsque de nouveaux renseignements deviennent disponibles. Il peut s'avérer nécessaire d'adapter la conception de l'étude (p. ex. le protocole expérimental) ou les mesures d'atténuation si une augmentation de la possibilité de double usage est identifiée.
4.5 Résultats
La responsabilité éthique des scientifiques s'étend à la phase de partage des résultats avec la communauté scientifique élargie ou le grand public. Les résultats d'un projet de recherche peuvent être évalués quant à leur possibilité de double usage avant leur soumission pour publication (p. ex. un manuscrit, un brevet), lors de l'examen par les pairs, ou même après leur publication. L'atténuation des risques associés à la possibilité de double usage à ce stade est plus efficace lorsque toutes les parties prenantes concernées collaborent à l'évaluation des résultats. Ceci peut comprendre la haute direction, des chercheurs, le CIB, des comités éditoriaux et des organismes de réglementation.
Retour en hautChapitre 5 - Références et ressources
Arrangement de Wassenaar. (1996). Arrangement de Wassenaar relatif aux contrôles des exportations d’armes conventionnelles et de biens et technologies à double usage. Consulté le 2026-03-11 à l'adresse https://www.wassenaar.org/fr/
Bureau des affaires de désarmement des Nations unies. (1975). Convention sur l'interdiction de la mise au point, de la fabrication et du stockage des armes bactériologiques (biologiques) ou à toxines et sur leur destruction. Consulté le 2026-01-07 à l'adresse https://front.un-arm.org/wp-content/uploads/2020/12/BWC-text-French.pdf
Cello, J., Paul, A. V. et Wimmer, E. (2002). Chemical Synthesis of Poliovirus cDNA: Generation of Infectious Virus in the Absence of Natural Template. Science, 297(5583): 1016-1018.
Centers for Disease Control and Prevention (États-Unis). (2005). Researchers Reconstruct 1918 Pandemic Influenza Virus; Effort Designed To Advance Preparedness. ScienceDaily. Consulté le 2026-01-07 à l'adresse https://www.sciencedaily.com/releases/2005/10/051005230557.htm
Cole, J., Morris, P., Dickman, M. J. et Dockrell, D. H. (2016). The Therapeutic Potential of Epigenetic Manipulation During Infectious Diseases. Pharmacology & Therapeutics, 167: 85-99.
Conseil de sécurité des Nations unies. (2004). Résolution 1540. Conseil de sécurité des Nations unies. Consulté le 2025-01-05 à l'adresse https://www.un.org/fr/sc/1540/resolutions-committee-reports-and-SC-briefings/security-council-resolutions.shtml
Debmalya, B., Vijender, C., Eugenia, C. Y., Emmanuel, O. S., Sudhir, C. et al. (2014). In Silico Models: From Simple Networks to Complex Diseases. Dans Ashish, S. V. et Anchal, S. (Éds.), Animal Biotechnology (p. 385-404). San Diego, Californie, États-Unis : Academic Press.
Federal Bureau of Investigation (États-Unis). Amerithrax. Consulté le 2026-01-07 à l'adresse https://vault.fbi.gov/Amerithrax
Gouvernement du Canada. (2015). Plan de surveillance administrative à l'égard des agents pathogènes et des toxines dans un contexte de recherche – Éléments requis et lignes directrices. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/biosecurite-biosurete-laboratoire/programme-delivrance-permis/plan-surveillance-administrative-a-egard-agents-pathogenes-toxines-contexte-recherche-elements-requis-lignes-directrices.html
Gouvernement du Canada. (2018). Ligne directrice canadienne sur la biosécurité – Effectuer une évaluation des risques de biosûreté. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/normes-lignes-directrices-canadiennes-biosecurite/directrices.html
Gouvernement du Canada. (2018). Ligne directrice canadienne sur la biosécurité – Évaluation des risques associés à l’agent pathogène. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/normes-lignes-directrices-canadiennes-biosecurite/directrices.html
Gouvernement du Canada. (2021). Politique sur la recherche scientifique avec les agents pathogènes humains et les toxines. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/biosecurite-biosurete-laboratoire/politique-recherche-scientifique-agents-pathogenes-humains-toxines.html
Gouvernement du Canada. (2022). Norme canadienne sur la biosécurité (3e éd.). Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/normes-lignes-directrices-canadiennes-biosecurite/troisieme-edition.html
Gouvernement du Canada. (2024). Addenda de biosûreté apporté à la Norme canadienne sur la biosécurité, troisième édition. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://training-formation.phac-aspc.gc.ca/mod/page/view.php?id=16281&lang=fr
Gouvernement du Canada. (2024). Domaines de recherche en technologies sensibles. Disponible à l'adresse https://science.gc.ca/site/science/fr/protegez-votre-recherche/lignes-directrices-outils-pour-mise-oeuvre-securite-recherche/recherche-technologies-sensibles-affiliations-preoccupantes/domaines-recherche-technologies-sensibles
Gouvernement du Canada. (2024). Énoncés de politique. Disponible à l'adresse https://science.gc.ca/site/science/fr/protegez-votre-recherche/renseignements-generaux-securite-recherche/ressources-supplementaires/enonces-politique
Gouvernement du Canada. (2024). La cybermenace ciblant des laboratoires de recherche. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.cyber.gc.ca/fr/orientation/cybermenace-ciblant-laboratoires-recherche
Gouvernement du Canada. (2024). Le Canada et le Règlement sanitaire international (RSI) : aperçu. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/mesures-interventions-urgence/reglement-sanitaire-international.html
Gouvernement du Canada. (2024). Organisations de recherche nommées. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://science.gc.ca/site/science/fr/protegez-votre-recherche/lignes-directrices-outils-pour-mise-oeuvre-securite-recherche/recherche-technologies-sensibles-affiliations-preoccupantes/organisations-recherche-nommees
Gouvernement du Canada. (2024). Politique sur la recherche en technologies sensibles et sur les affiliations préoccupantes. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://science.gc.ca/site/science/fr/protegez-votre-recherche/lignes-directrices-outils-pour-mise-oeuvre-securite-recherche/recherche-technologies-sensibles-affiliations-preoccupantes/politique-recherche-technologies-sensibles-affiliations-preoccupantes
Gouvernement du Canada. (2025). Guide de la Liste des marchandises et technologies d’exportation contrôlée du Canada. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.international.gc.ca/trade-commerce/controls-controles/ecl-lec/index.aspx?lang=fra
Gouvernement du Canada. (2025). Lignes directrices sur la sécurité nationale pour les partenariats de recherche. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://science.gc.ca/site/science/fr/protegez-votre-recherche/lignes-directrices-outils-pour-mise-oeuvre-securite-recherche/lignes-directrices-securite-nationale-pour-partenariats-recherche
Gouvernement du Canada. (2025). Liste de technologies sensibles. Disponible à l'adresse https://www.canada.ca/fr/services/defense/securitenationale/liste-technologies-sensibles.html
Groupe d'Australie. (2023). Liste des agents pathogènes humains et animaux et des toxines réglementes à l'exportation. Consulté le 2026-03-11 à l'adresse https://www.dfat.gov.au/publications/minisite/theaustraliagroupnet/site/fr/human_animal_pathogens.html
Herfst, S., Schrauwen, E. J., Linster, M., Chutinimitkul, S., de Wit, E. et al. (2012). Airborne Transmission of Influenza A/H5N1 Virus Between Ferrets. Science, 336(6088): 1534-1541.
Imai, M., Watanabe, T., Hatta, M., Das, S. C., Ozawa, M. et al. (2012). Experimental Adaptation of an Influenza H5 HA Confers Respiratory Droplet Transmission to a Reassortant H5 HA/H1N1 Virus in Ferrets. Nature, 486(7403): 420-428.
Licht, J. D. et Bennett, R. L. (2021). Leveraging Epigenetics to Enhance the Efficacy of Immunotherapy. Clinical Epigenetics, 13(1): 115.
Liste des marchandises et technologies d’exportation contrôlée (DORS/89-202).
Loi sur la santé des animaux (L.C. 1990, ch. 21).
Loi sur les agents pathogènes humains et les toxines (L.C. 2009, ch. 24).
Loi sur les licences d’exportation et d’importation (L.R.C., 1985, ch. E-19).
Mansfield, M. J., Wentz, T. G., Zhang, S., Lee, E. J., Dong, M. et al. (2019). Bioinformatic Discovery of a Toxin Family in Chryseobacterium piperi with Sequence Similarity to Botulinum Neurotoxins. Science Reports, 9(1): 1634.
McMullan, L. K., Flint, M., Chakrabarti, A., Guerrero, L., Lo, M. K. et al. (2019). Characterisation of Infectious Ebola Virus from the Ongoing Outbreak to Guide Response Activities in the Democratic Republic of the Congo: A Phylogenetic and In Vitro Analysis. The Lancet Infectious Diseases, 19(9): 1023-1032.
National Academies of Sciences, Engineering and Medicine (États-Unis). (2017). Managing Dual Use Research of Concern. Dans Dual Use Research of Concern in the Life Sciences: Current Issues and Controversies (p. 45-72). Washington, DC, États-Unis : National Academies Press.
National Research Council of the National Academies (États-Unis). (2015). Gain-of-Function Research: Background and Alternatives. Dans Potential Risks and Benefits of Gain-of-Function Research: Summary of a Workshop (p. 21-28). Washington, DC, États-Unis : National Academies Press.
Negi, S. S., Schein, C. H., Ladics, G. S., Mirsky, H., Chang, P. et al. (2017). Functional Classification of Protein Toxins as a Basis for Bioinformatic Screening. Scientific Reports, 7(1): 13940.
Noyce, R. S., Lederman, S. et Evans, D. H. (2018). Construction of an Infectious Horsepox Virus Vaccine from Chemically Synthesized DNA Fragments. Public Library of Science One, 13(1): e0188453.
Organisation internationale de normalisation. (2020). ISO 35001:2019, Système de management des biorisques pour les laboratoires et autres organismes associés. Genève, Suisse : Organisation internationale de normalisation.
Organisation mondiale de la Santé. (2016). Règlement sanitaire international (2005) (3e éd.). Genève, Suisse : Éditions de l'OMS.
Organisation mondiale de la Santé. (2022). Cadre d’orientation mondial pour l’usage responsable des sciences de la vie : Atténuer les risques biologiques et régir la recherche duale. Organisation mondiale de la Santé. Consulté le 2026-03-16 à l'adresse https://www.who.int/fr/publications/i/item/9789240056107
Organisation mondiale de la Santé. (2024). Laboratory Biosecurity Guidance. Organisation mondiale de la Santé. Consulté le 2025-06-11 à l'adresse https://www.who.int/fr/publications/i/item/9789240095113
Organisation mondiale de la Santé. (2025). International Health Regulations. Consulté le 2025-06-11 à l'adresse https://www.who.int/health-topics/international-health-regulations/#tab=tab_2
Règlement sur la santé des animaux (C.R.C., ch. 296).
Règlement sur les agents pathogènes humains et les toxines (DORS/2015-44).
Rosengard, A. M., Liu, Y., Nie, Z. et Jimenez, R. (2002). Variola Virus Immune Evasion Design: Expression of a Highly Efficient Inhibitor of Human Complement. Proceedings of the National Academy of Sciences of the United States of America, 99(13): 8808-8813.
Satyanarayana, K. (2011). Dual Dual-Use Research of Concern: Publish and Perish? Indian Journal of Medical Research, 133(1): 1-4.
Schuerger, C., Batalis, S., Quinn, K., Kinoshita, R., Daniels, O. J. et Puglisi, A. (2023). Understanding the Global Gain-of-Function Research Landscape. Center for Security and Emerging Technology. Consulté le 2025-05-22 à l'adresse https://cset.georgetown.edu/publication/understanding-the-global-gain-of-function-research-landscape/
Tumpey, T. M., Basler, C. F., Aguilar, P. V., Zeng, H., Solórzano, A. et al. (2005). Characterization of the Reconstructed 1918 Spanish Influenza Pandemic Virus. Science, 310(5745): 77-80.
Urbina, F., Lentzos, F., Invernizzi, C. et Ekins, S. (2022). Dual Use of Artificial-Intelligence-Powered Drug Discovery. Nature Machine Intelligence, 4(3): 189-191.
Warrick, J. (2010). FBI Investigation of 2001 Anthrax Attacks Concluded; U.S. Releases Details. Washington Post. Consulté le 2026-01-07 à l'adresse https://www.washingtonpost.com/wp-dyn/content/article/2010/02/19/AR2010021902369.html
Wishart, D., Arndt, D., Pon, A., Sajed, T., Guo, A. C. et al. (2015). T3DB: the Toxic Exposome Database. Nucleic Acids Research, 43(Database issue): D928-934.
Xie, X., Lokugamage, K. G., Zhang, X., Vu, M. N., Muruato, A. E. et al. (2021). Engineering SARS-CoV-2 Using a Reverse Genetic System. Nature Protocols, 16(3): 1761-1784.
Zarzeczny, A. et Caulfield, T. (2009). Emerging Ethical, Legal and Social Issues Associated with Stem Cell Research and the Current Role of the Moral Status of the Embryo. Stem Cell Reviews and Reports, 5(2): 96-101.
Ressources supplémentaires
Biosecurity Office (Pays-Bas). Dual-Use Quickscan. Consulté le 2026-01-07 à l'adresse https://dualusequickscan.com/en/
Georgetown University. Biosecurity Central. Consulté le 2026-01-07 à l'adresse https://www.biosecuritycentral.org/
Gouvernement du Canada. Orientations des trois organismes concernant la sécurité de la recherche. Disponible à l'adresse https://www.nserc-crsng.gc.ca/InterAgency-Interorganismes/RS-SR/index_fra.asp
Gouvernement du Canada. (2016). Ligne directrice canadienne sur la biosécurité – Élaboration d'un plan de biosûreté exhaustif. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/normes-lignes-directrices-canadiennes-biosecurite/directrices.html
Gouvernement du Canada. (2017). Ligne directrice canadienne sur la biosécurité – Notification et déclaration en vertu de la LAPHT et du RAPHT. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/normes-lignes-directrices-canadiennes-biosecurite/directrices.html
Gouvernement du Canada. (2018). Ligne directrice canadienne sur la biosécurité – Évaluation locale des risques. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/normes-lignes-directrices-canadiennes-biosecurite/directrices.html
Gouvernement du Canada. (2022). Gestion efficace du double usage dans le domaine de la recherche en sciences de la vie. Disponible à l'adresse https://training-formation.phac-aspc.gc.ca/course/info.php?id=493&lang=fr
Gouvernement du Canada. (2022). Protégez votre recherche. Disponible à l'adresse https://science.gc.ca/site/science/fr/protegez-votre-recherche
Gouvernement du Canada. (2023). Introduction à la biosûreté. Disponible à l'adresse https://training-formation.phac-aspc.gc.ca/enrol/index.php?id=6
Gouvernement du Canada. (2023). Introduction au double usage dans les recherches en science de la vie. Disponible à l'adresse https://training-formation.phac-aspc.gc.ca/course/view.php?id=110&lang=fr
Gouvernement du Canada. (2023). Mémorandum D19-9-4 : Importation et exportation d'agents pathogènes et de toxines. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.cbsa-asfc.gc.ca/publications/dm-md/d19/d19-9-4-fra.html
Gouvernement du Canada. (2024). Biosûreté. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/biosecurite-biosurete-laboratoire/biosecurite.html
Gouvernement du Canada. (2024). Sécurité de la recherche. Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/services/defense/securiterecherche/apropos.html
Gouvernement du Canada. (2024). Webinaire sur la science en sécurité (le 19 juin 2024). Disponible à l'adresse https://training-formation.phac-aspc.gc.ca/enrol/index.php?id=712
Gouvernement du Canada. (2025). Science en sécurité. Disponible à l'adresse https://www.securitepublique.gc.ca/cnt/ntnl-scrt/cntr-trrrsm/cntr-prlfrtn/sfgrdng-scnc/sfgrdng-scnc-wrkshp-fr.aspx
Organisation mondiale de la Santé. Ensuring responsible use of life sciences research. Consulté le 2025-07-16 à l'adresse https://www.who.int/activities/ensuring-responsible-use-of-life-sciences-research
Retour en hautAnnexe A – Initiatives internationales relatives à la possibilité de double usage
Le Canada participe à de multiples initiatives internationales de contrôle des biens à double usage, lesquelles se reflètent dans la législation et les politiques canadiennes. De nombreuses initiatives internationales visent à identifier et à atténuer les risques associés à la recherche biologique, et fournissent le contexte mondial actuel sur la possibilité de double usage.
Groupe d'Australie
Le Groupe d'Australie est un arrangement informel qui vise à harmoniser les contrôles à l'exportation afin de prévenir que les exportations ne contribuent au développement et à la prolifération d'armes chimiques et biologiques. Il a été créé en 1985 et compte 43 pays membres, dont le Canada. Dans les années 1990, les agents biologiques présentant une possibilité de double usage ont été ajoutés aux listes de contrôle à l’exportation élaborées par le Groupe d'Australie. Le Canada met en œuvre la liste de contrôle commune du Groupe d'Australie intitulée Liste des agents pathogènes humains et animaux et des toxines réglementés à l’exportation par le biais de la Loi sur les licences d'exportation et d'importationNote de bas de page22. De plus, cette liste de contrôle commune est incorporée par référence dans le RAPHT en tant que critère pour un agent pathogène humain ou une toxine précisé (c.-à-d. un ABCSE) au CanadaNote de bas de page46.
Convention sur les armes biologiques
Au niveau international, depuis 1975, les États parties se sont engagés à ne pas délibérément mettre au point d'agents microbiologiques en tant qu'armes biologiques dans le cadre de la Convention sur l'interdiction de la mise au point, de la fabrication et du stockage des armes bactériologiques (biologiques) ou à toxines et sur leur destruction. Particulièrement, l'Article premier de la Convention stipule ce qui suit :
« Chaque État partie à la présente Convention s'engage à ne jamais, et en aucune circonstance, mettre au point, fabriquer, stocker, ni acquérir d’une manière ou d’une autre ni conserver :
1) des agents microbiologiques ou autres agents biologiques, ainsi que des toxines quels qu’en soient l’origine ou le mode de production, de types et en quantités qui ne sont pas destinés à des fins prophylactiques, de protection ou à d’autres fins pacifiques;
2) des armes, de l’équipement ou des vecteurs destinés à l’emploi de tels agents ou toxines à des fins hostiles ou dans des conflits armésNote de bas de page47. »
La Convention est un élément clé des efforts déployés par la communauté internationale pour lutter contre la prolifération des armes de destruction massive. Elle a été adoptée par 188 États, dont le Canada.
Règlement sanitaire international
Le Règlement sanitaire international (RSI) impose à 196 pays, dont le Canada, de travailler ensemble pour prévenir la propagation internationale des maladies, s’en protéger, la maîtriser et y réagir sans entraver inutilement le trafic et le commerce internationauxNote de bas de page48. Le RSI fournit un cadre pour la gestion des événements et des urgences possibles en matière de santé publique internationale. Les pays sont tenus d'élaborer, de renforcer et de maintenir des capacités fondamentales spécifiques comprenant les éléments suivantsNote de bas de page49 :
- la surveillance nationale pour détecter les menaces possibles pour la santé publique
- l’évaluation des événements de santé publique sur leur territoire
- la notification et la déclaration à l'OMS des événements de santé publique survenant sur leur territoire qui peuvent constituer une urgence de santé publique de portée internationale
- l’intervention en cas de risques et d'urgences pour la santé publique
De plus, dans la mesure du possible, les pays sont tenus de déclarer à l'OMS dans les 24 heures suivant la réception de preuves d'un risque pour la santé publique identifié en dehors de leur territoire qui pourrait entraîner une propagation internationale d’une maladieNote de bas de page50.
Résolution 1540 du Conseil de sécurité des Nations Unies
La Résolution 1540 du Conseil de sécurité des Nations Unies a été adoptée en 2004 afin de prévenir la mise au point d'armes biologiques et d'autres armes et des éléments connexesNote de bas de page51. La résolution exige que les 193 États membres des Nations Unies adoptent et appliquent des lois appropriées à cet effet ainsi que d'autres mesures efficaces pour prévenir la prolifération de ces armes et de leurs vecteurs afin d'empêcher les acteurs non étatiques d'y avoir accès, en particulier à des fins terroristes. Les membres des Nations Unies, dont le Canada, doivent rendre compte de leur respect de cette obligation.
Le comité du Conseil de sécurité qui a été créé conformément à la Résolution 1540 est responsable de faire rapport au Conseil de sécurité sur la mise en œuvre de cette résolution. Le Bureau des affaires de désarmement des Nations Unies (UNODA) appuie les activités de ce comité et vise à promouvoir les efforts multilatéraux dans le but de parvenir à un désarmement complet. Cela comprend :
- l’appui à la coopération régionale pour faciliter les activités de mise en œuvre au niveau national
- la promotion de la coopération entre les organisations internationales, régionales et sous-régionales
- le fait de cultiver des partenariats efficaces entre les principales parties prenantes, y compris la société civile, le secteur privé et le monde universitaire
Arrangement de Wassenaar
L'Arrangement de Wassenaar relatif au contrôle des exportations d'armes conventionnelles et de biens et technologies à double usage, communément appelé l'Arrangement de Wassenaar, a été établi en 1996. L'un de ses objectifs est de contribuer à la sécurité et à la stabilité régionales et internationales en encourageant la transparence volontaire et une plus grande responsabilité dans les transferts d'armes conventionnelles et de biens et technologies à double usage, prévenant ainsi les accumulations déstabilisatricesNote de bas de page52. Les États participants s'efforcent, par le biais de leurs politiques nationales, de veiller à ce que les transferts de ces biens ne contribuent pas au développement ou au renforcement de capacités militaires qui compromettent les objectifs de l'arrangement, et à ce qu'ils ne soient pas détournés pour appuyer de telles capacités. Il y a actuellement 42 États participants, dont le Canada.
Organisation mondiale de la Santé
Avec 194 États membres, l'un des objectifs de l’OMS est de promouvoir une recherche responsable et innovante dans le domaine des sciences de la vie au niveau mondial. Elle y parvient par divers moyens, notamment en organisant des événements, des réunions et des ateliers, et en publiant des documents d'orientation et des bulletins d'information. Par exemple, l'OMS a publié des documents d’orientation et des cadres en matière de gestion efficace des risques et de biosûreté en laboratoire. L'OMS qualifie de « recherche à haut risque » la recherche sur des matières biologiques qui pourraient avoir des conséquences graves ou catastrophiques pour la vieNote de bas de page53.
Retour en hautRéférences
- Note de bas de page 1
-
Organisation mondiale de la Santé. (2022). Cadre d’orientation mondial pour l’usage responsable des sciences de la vie : Atténuer les risques biologiques et régir la recherche duale. Organisation mondiale de la Santé. Consulté le 2026-03-16 à l'adresse https://www.who.int/fr/publications/i/item/9789240056107
- Note de bas de page 2
-
National Academies of Sciences, Engineering and Medicine (États-Unis). (2017). Managing Dual Use Research of Concern. Dans Dual Use Research of Concern in the Life Sciences: Current Issues and Controversies (p. 45-72). Washington, DC, États-Unis : National Academies Press.
- Note de bas de page 3
-
Federal Bureau of Investigation (États-Unis). Amerithrax. Consulté le 2026-01-07 à l'adresse https://vault.fbi.gov/Amerithrax
- Note de bas de page 4
-
Warrick, J. (2010). FBI Investigation of 2001 Anthrax Attacks Concluded; U.S. Releases Details. Washington Post. Consulté le 2026-01-07 à l'adresse https://www.washingtonpost.com/wp-dyn/content/article/2010/02/19/AR2010021902369.html
- Note de bas de page 5
-
Satyanarayana, K. (2011). Dual Dual-Use Research of Concern: Publish and Perish? Indian Journal of Medical Research, 133(1): 1-4.
- Note de bas de page 6
-
Zarzeczny, A. et Caulfield, T. (2009). Emerging Ethical, Legal and Social Issues Associated with Stem Cell Research and the Current Role of the Moral Status of the Embryo. Stem Cell Reviews and Reports, 5(2): 96-101.
- Note de bas de page 7
-
National Research Council of the National Academies (États-Unis). (2015). Gain-of-Function Research: Background and Alternatives. Dans Potential Risks and Benefits of Gain-of-Function Research: Summary of a Workshop (p. 21-28). Washington, DC, États-Unis : National Academies Press.
- Note de bas de page 8
-
Cello, J., Paul, A. V. et Wimmer, E. (2002). Chemical Synthesis of Poliovirus cDNA: Generation of Infectious Virus in the Absence of Natural Template. Science, 297(5583): 1016-1018.
- Note de bas de page 9
-
Rosengard, A. M., Liu, Y., Nie, Z. et Jimenez, R. (2002). Variola Virus Immune Evasion Design: Expression of a Highly Efficient Inhibitor of Human Complement. Proceedings of the National Academy of Sciences of the United States of America, 99(13): 8808-8813.
- Note de bas de page 10
-
Tumpey, T. M., Basler, C. F., Aguilar, P. V., Zeng, H., Solórzano, A. et al. (2005). Characterization of the Reconstructed 1918 Spanish Influenza Pandemic Virus. Science, 310(5745): 77-80.
- Note de bas de page 11
-
Centers for Disease Control and Prevention (États-Unis). (2005). Researchers Reconstruct 1918 Pandemic Influenza Virus; Effort Designed To Advance Preparedness. ScienceDaily. Consulté le 2026-01-07 à l'adresse https://www.sciencedaily.com/releases/2005/10/051005230557.htm
- Note de bas de page 12
-
Imai, M., Watanabe, T., Hatta, M., Das, S. C., Ozawa, M. et al. (2012). Experimental Adaptation of an Influenza H5 HA Confers Respiratory Droplet Transmission to a Reassortant H5 HA/H1N1 Virus in Ferrets. Nature, 486(7403): 420-428.
- Note de bas de page 13
-
Herfst, S., Schrauwen, E. J., Linster, M., Chutinimitkul, S., de Wit, E. et al. (2012). Airborne Transmission of Influenza A/H5N1 Virus Between Ferrets. Science, 336(6088): 1534-1541.
- Note de bas de page 14
-
Noyce, R. S., Lederman, S. et Evans, D. H. (2018). Construction of an Infectious Horsepox Virus Vaccine from Chemically Synthesized DNA Fragments. Public Library of Science One, 13(1): e0188453.
- Note de bas de page 15
-
McMullan, L. K., Flint, M., Chakrabarti, A., Guerrero, L., Lo, M. K. et al. (2019). Characterisation of Infectious Ebola Virus from the Ongoing Outbreak to Guide Response Activities in the Democratic Republic of the Congo: A Phylogenetic and In Vitro Analysis. The Lancet Infectious Diseases, 19(9): 1023-1032.
- Note de bas de page 16
-
Xie, X., Lokugamage, K. G., Zhang, X., Vu, M. N., Muruato, A. E. et al. (2021). Engineering SARS-CoV-2 Using a Reverse Genetic System. Nature Protocols, 16(3): 1761-1784.
- Note de bas de page 17
-
Loi sur les agents pathogènes humains et les toxines (L.C. 2009, ch. 24).
- Note de bas de page 18
-
Règlement sur les agents pathogènes humains et les toxines (DORS/2015-44).
- Note de bas de page 19
-
Loi sur la santé des animaux (L.C. 1990, ch. 21).
- Note de bas de page 20
-
Règlement sur la santé des animaux (C.R.C., ch. 296).
- Note de bas de page 21
-
Gouvernement du Canada. (2022). Norme canadienne sur la biosécurité (3e éd.). Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/normes-lignes-directrices-canadiennes-biosecurite/troisieme-edition.html
- Note de bas de page 22
-
Loi sur les licences d’exportation et d’importation (L.R.C., 1985, ch. E-19).
- Note de bas de page 23
-
Liste des marchandises et technologies d’exportation contrôlée (DORS/89-202).
- Note de bas de page 24
-
Gouvernement du Canada. (2025). Guide de la Liste des marchandises et technologies d’exportation contrôlée du Canada. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.international.gc.ca/trade-commerce/controls-controles/ecl-lec/index.aspx?lang=fra
- Note de bas de page 25
-
Gouvernement du Canada. (2021). Politique sur la recherche scientifique avec les agents pathogènes humains et les toxines. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/biosecurite-biosurete-laboratoire/politique-recherche-scientifique-agents-pathogenes-humains-toxines.html
- Note de bas de page 26
-
Gouvernement du Canada. (2015). Plan de surveillance administrative à l'égard des agents pathogènes et des toxines dans un contexte de recherche – Éléments requis et lignes directrices. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/biosecurite-biosurete-laboratoire/programme-delivrance-permis/plan-surveillance-administrative-a-egard-agents-pathogenes-toxines-contexte-recherche-elements-requis-lignes-directrices.html
- Note de bas de page 27
-
Gouvernement du Canada. (2025). Liste de technologies sensibles. Disponible à l'adresse https://www.canada.ca/fr/services/defense/securitenationale/liste-technologies-sensibles.html
- Note de bas de page 28
-
Urbina, F., Lentzos, F., Invernizzi, C. et Ekins, S. (2022). Dual Use of Artificial-Intelligence-Powered Drug Discovery. Nature Machine Intelligence, 4(3): 189-191.
- Note de bas de page 29
-
Schuerger, C., Batalis, S., Quinn, K., Kinoshita, R., Daniels, O. J. et Puglisi, A. (2023). Understanding the Global Gain-of-Function Research Landscape. Center for Security and Emerging Technology. Consulté le 2025-05-22 à l'adresse https://cset.georgetown.edu/publication/understanding-the-global-gain-of-function-research-landscape/
- Note de bas de page 30
-
Licht, J. D. et Bennett, R. L. (2021). Leveraging Epigenetics to Enhance the Efficacy of Immunotherapy. Clinical Epigenetics, 13(1): 115.
- Note de bas de page 31
-
Cole, J., Morris, P., Dickman, M. J. et Dockrell, D. H. (2016). The Therapeutic Potential of Epigenetic Manipulation During Infectious Diseases. Pharmacology & Therapeutics, 167: 85-99.
- Note de bas de page 32
-
Wishart, D., Arndt, D., Pon, A., Sajed, T., Guo, A. C. et al. (2015). T3DB: the Toxic Exposome Database. Nucleic Acids Research, 43(Database issue): D928-934.
- Note de bas de page 33
-
Negi, S. S., Schein, C. H., Ladics, G. S., Mirsky, H., Chang, P. et al. (2017). Functional Classification of Protein Toxins as a Basis for Bioinformatic Screening. Scientific Reports, 7(1): 13940.
- Note de bas de page 34
-
Mansfield, M. J., Wentz, T. G., Zhang, S., Lee, E. J., Dong, M. et al. (2019). Bioinformatic Discovery of a Toxin Family in Chryseobacterium piperi with Sequence Similarity to Botulinum Neurotoxins. Science Reports, 9(1): 1634.
- Note de bas de page 35
-
Gouvernement du Canada. (2018). Ligne directrice canadienne sur la biosécurité – Évaluation des risques associés à l’agent pathogène. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/normes-lignes-directrices-canadiennes-biosecurite/directrices.html
- Note de bas de page 36
-
Gouvernement du Canada. (2024). La cybermenace ciblant des laboratoires de recherche. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.cyber.gc.ca/fr/orientation/cybermenace-ciblant-laboratoires-recherche
- Note de bas de page 37
-
Gouvernement du Canada. (2024). Énoncés de politique. Disponible à l'adresse https://science.gc.ca/site/science/fr/protegez-votre-recherche/renseignements-generaux-securite-recherche/ressources-supplementaires/enonces-politique
- Note de bas de page 38
-
Gouvernement du Canada. (2018). Ligne directrice canadienne sur la biosécurité – Effectuer une évaluation des risques de biosûreté. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/normes-lignes-directrices-canadiennes-biosecurite/directrices.html
- Note de bas de page 39
-
Organisation internationale de normalisation. (2020). ISO 35001:2019, Système de management des biorisques pour les laboratoires et autres organismes associés. Genève, Suisse : Organisation internationale de normalisation.
- Note de bas de page 40
-
Gouvernement du Canada. (2024). Addenda de biosûreté apporté à la Norme canadienne sur la biosécurité, troisième édition. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://training-formation.phac-aspc.gc.ca/mod/page/view.php?id=16281&lang=fr
- Note de bas de page 41
-
Debmalya, B., Vijender, C., Eugenia, C. Y., Emmanuel, O. S., Sudhir, C. et al. (2014). In Silico Models: From Simple Networks to Complex Diseases. Dans Ashish, S. V. et Anchal, S. (Éds.), Animal Biotechnology (p. 385-404). San Diego, Californie, États-Unis : Academic Press.
- Note de bas de page 42
-
Gouvernement du Canada. (2024). Politique sur la recherche en technologies sensibles et sur les affiliations préoccupantes. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://science.gc.ca/site/science/fr/protegez-votre-recherche/lignes-directrices-outils-pour-mise-oeuvre-securite-recherche/recherche-technologies-sensibles-affiliations-preoccupantes/politique-recherche-technologies-sensibles-affiliations-preoccupantes
- Note de bas de page 43
-
Gouvernement du Canada. (2025). Lignes directrices sur la sécurité nationale pour les partenariats de recherche. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://science.gc.ca/site/science/fr/protegez-votre-recherche/lignes-directrices-outils-pour-mise-oeuvre-securite-recherche/lignes-directrices-securite-nationale-pour-partenariats-recherche
- Note de bas de page 44
-
Gouvernement du Canada. (2024). Domaines de recherche en technologies sensibles. Disponible à l'adresse https://science.gc.ca/site/science/fr/protegez-votre-recherche/lignes-directrices-outils-pour-mise-oeuvre-securite-recherche/recherche-technologies-sensibles-affiliations-preoccupantes/domaines-recherche-technologies-sensibles
- Note de bas de page 45
-
Gouvernement du Canada. (2024). Organisations de recherche nommées. Ottawa, ON, Canada : Gouvernement du Canada. Disponible à l'adresse https://science.gc.ca/site/science/fr/protegez-votre-recherche/lignes-directrices-outils-pour-mise-oeuvre-securite-recherche/recherche-technologies-sensibles-affiliations-preoccupantes/organisations-recherche-nommees
- Note de bas de page 46
-
Groupe d'Australie. (2023). Liste des agents pathogènes humains et animaux et des toxines réglementes à l'exportation. Consulté le 2026-03-11 à l'adresse https://www.dfat.gov.au/publications/minisite/theaustraliagroupnet/site/fr/human_animal_pathogens.html
- Note de bas de page 47
-
Bureau des affaires de désarmement des Nations unies. (1975). Convention sur l'interdiction de la mise au point, de la fabrication et du stockage des armes bactériologiques (biologiques) ou à toxines et sur leur destruction. Consulté le 2026-01-07 à l'adresse https://front.un-arm.org/wp-content/uploads/2020/12/BWC-text-French.pdf
- Note de bas de page 48
-
Gouvernement du Canada. (2024). Le Canada et le Règlement sanitaire international (RSI) : aperçu. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/mesures-interventions-urgence/reglement-sanitaire-international.html
- Note de bas de page 49
-
Organisation mondiale de la Santé. (2025). International Health Regulations. Consulté le 2025-06-11 à l'adresse https://www.who.int/health-topics/international-health-regulations/#tab=tab_2
- Note de bas de page 50
-
Organisation mondiale de la Santé. (2016). Règlement sanitaire international (2005) (3e éd.). Genève, Suisse : Éditions de l'OMS.
- Note de bas de page 51
-
Conseil de sécurité des Nations unies. (2004). Résolution 1540. Conseil de sécurité des Nations unies. Consulté le 2025-01-05 à l'adresse https://www.un.org/fr/sc/1540/resolutions-committee-reports-and-SC-briefings/security-council-resolutions.shtml
- Note de bas de page 52
-
Arrangement de Wassenaar. (1996). Arrangement de Wassenaar relatif aux contrôles des exportations d’armes conventionnelles et de biens et technologies à double usage. Consulté le 2026-03-11 à l'adresse https://www.wassenaar.org/fr/
- Note de bas de page 53
-
Organisation mondiale de la Santé. (2024). Laboratory Biosecurity Guidance. Organisation mondiale de la Santé. Consulté le 2025-06-11 à l'adresse https://www.who.int/fr/publications/i/item/9789240095113
